生物酶催化技术及应用
酶是非常强大的催化剂,它使用复杂的活性位点来处理化学转化。酶强大的加速反应能力和无与伦比的选择性使它们成为可用于可持续制造过程的有吸引力的催化剂。生物催化领域已经发展到现在被视为发展更绿色、更高效化学工业的关键赋能技术的阶段。几项重大方法创新支撑了快速进展,包括:
1) 提供快速、准确和低成本的DNA合成和测序服务;
2) 开发先进的生物信息学工具和计算建模方法;
3) 以及用于高通量结构和生化酶表征的日益复杂的实验工作流程。
然而由于生物系统本身的复杂性及天然酶对非天然产品的适用性较差,生物催化工艺的开发往往周期漫长,投入巨大,这严重限制了生物催化技术的推广。天然酶,通常需要蛋白质工程来优化其特性以用于实际应用。近年来,出现了高通量蛋白质工程策略,最显著的是定向进化,用于开发生物催化剂,以高效和选择性地处理非天然底物,并在商业可行的工艺条件下有效运行。
生物体内催化
生物体内催化在活的宿主细胞里进行,通过多种酶有机的结合,按照代谢途径一步步进行催化反应。而代谢工程则是对这些代谢途径进行设计与构建,来更高效地获得产物。由于在活细胞内的生物转换不需要外源辅助因子的补充,也不需要进行蛋白质纯化等步骤,体内催化成为一种成本效益很高的方法。
体内发酵与代谢工程代谢工程利用分子生物学技术或基因工程例如DNA重组技术,通过操控细胞内的酶、运输和调节功能等,来改变或构建细胞的活动和代谢途径,从而提高所需产物的产量或得到新产物[1]。一个成功的代谢工程基于对细胞功能的分析设计出改进的菌株,再通过基因工程进行构建。随着对代谢工程的研究越来越多,很多人都以自身对其的理解对代谢工程进行了分类[1,2],其中Nielsen J.根据不同的方法和目的对生物代谢工程进行了细分[3]:1、将异源基因插入宿主中来生产异源蛋白;2、为了更有效地利用原料而扩大微生物对底物的应用范围;3、通过基因洗牌或蛋白质定向进化等策略生产全新的代谢途径,从而提高生成速率;4、通过插入其他生物的代谢途径,使特定生物体拥有能同时降解多种化合物的能力;5、为改进细胞理化性质、形态,而对细胞生理学进行工程设计;6、为避免副产物对细胞造成负面影响而设计代谢途径,从而消除或减少副产物的生成;7、通过增加生物合成途径的活性而增加产量及生产力。
生物体外催化
生物体外催化则能通过对多个酶在实际生产条件下的性能进行工程化改造,多个酶同时参与级联反应来简化工艺流程,减少了一些中间产物或副产物的产生,避免了副产物对细胞的毒害,中间产物的分离,提高收率与纯度,同时节省了生产成本[4]。
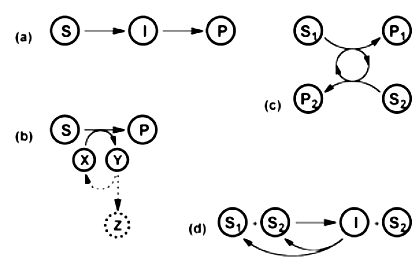
酶催化级联反应体系有多种类型,目前最通用的是分为以下四类[5]:(A)线性级联反应; (B)正交级联反应; (C)平行级联反应; (D)循环级联反应。实际的级联反应中,通常不会只应用一种反应类型,而是多类结合应用,氧化还原酶、转氨酶等则是其中最常应用的酶类。
A. 单个底物经酶催化为一个或多个中间物后转化为单个最终产物的过程称为线性级联反应,它是四种级联体系中最简单直观的;
B. 正交级联反应的特点在于酶将底物转化为产物后在辅助底物存在时参与另一种酶的反应以便辅因子或辅助底物再生,或是能够移除生成的副产物,使反应向正方向进行。最经典的正交级联是羰基还原酶偶联脱氢酶从而实现辅酶再生;
C. 两种及以上底物经不同生物催化反应体系转化为两种以上产物,但其共用同一套辅酶或辅底物再生系统的过程称为平行级联;
D. 循环级联反应即多个底物可选择性地被转化为一个中间物,随后又转化为所需化合物或者最初原料进行重复循环反应,在循环过程中所需化合物被不断积累。
体内与体外对比及优劣势分析
体内生物转化
优势:
1、体内可实现辅酶循环(如ATP,NADPH, SAM等),无需额外补充;
2、体内内环境稳定,相关酶的活性及稳定性不易受影响。
劣势:
1、合成在细胞内的代谢途径活跃的化合物会限制其积累浓度(如丙酮酸),即容易转化为其他物质,导致最终产率不高;
2、不易合成对细胞有毒性的化合物;
3、代谢通路的动力学不易控制和改造;
4、产物浓度通常较低,分离纯化比较复杂;
需要平衡产物生产通路和细胞生存通路对物质的竞争。
体外酶级联
优势:
1、减少反应步骤,降低成本;
2、可以针对产品的物理化学特性和分离工艺的要求灵活地选择反应体系,更易进行系统的工艺优化,能够达到很高的时空产率和提取收率。
3、可以选择适合的大宗品作为起始原料,能够达到最高的原子经济性(100%)。
劣势:
1、需要用到ATP,NADPH等价格昂贵的辅酶时,需同时考虑辅酶循环体系的构建;
2、部分酶在体外的稳定性较差,大规模稳定生产存在困难;
3、体外多酶的协作往往不如在体内有序高效。
生物酶催化技术在药物合成中的应用
在解决制药行业环境问题过程中,有多种生物催化剂可用于药物和药物中间体的合成,包括氧化酶、还原酶、水解酶、裂解酶、异构酶和转氨酶等。本文以最为常见的氧化反应和还原反应为例,简述生物酶催化技术在药物合成中的应用。
氧化反应
生物氧化反应目前已被广泛用于制药行业,人们正越来越多地探索将氧化酶用于生物催化。例如,丙肝病毒蛋白酶抑制剂telaprevir和boceprevir以及质子泵抑制剂埃索美拉唑在工业生产中都使用了氧化酶。又如,植物雌激素松脂醇在多种疾病过程中都能对机体起到保护作用,因此制药界对它的研究颇多。有报道称利用青霉菌(Penicillium simplicissimum)的香草醇氧化酶和细菌漆酶,使用价格低廉的丁子香酚做为起始原料,用两步一锅法合成松脂醇。在优化的条件下,松脂醇的合成可以达到1.6g/L的半制备规模(图2)。

图2. 利用香草醇氧化酶和细菌漆酶通过串联反应合成松脂醇
还原反应
使用生物酶催化剂对羰基官能团的区域选择性和立体选择性具有很好的效果,尤其是在还原合成手性药物中间体过程中具有重要意义。例如新的微生物菌株从环境中被分离出来,它们具有良好的羰基还原活性以及所需的生化特性,包括热稳定性和对有机溶剂的耐受性。
光学纯的叔丁基6-氰基-(3R,5R)-二羟基己酸酯是立普妥(阿托伐他汀钙)的关键手性前体,是由6-氰基-(5R)-羟基-3-氧代己酸叔丁酯通过还原酶还原生成的。有报道称在乳酸克鲁维酵母(Kluyveromyces lactis)中发现了一种新的羰基还原酶KlAKR,能够不对称还原6-氰基-(5R)-羟基-3-氧代己酸叔丁酯(图3)。并利用半理性设计策略改善酶的活性,经过两轮基于同源建模和分子对接的位点饱和突变筛选得到的突变体Y295W/W296L,催化效率比野生型KlAKR高11.25倍。

图3. 还原酶KlAKR催化的还原反应
通过筛选新的微生物,或通过基因组挖掘鉴别出新的基因,然后再通过强大的酶工程工具,包括理性设计、非理性设计、高通量筛选平台等对这些生物酶进行优化和筛选,不断开发新的酶催化剂。不仅开发出新的酶还要找到发挥其活性的环境并应用到合适的反应中去。
生物酶的研究前景
过去十年酶设计和工程领域取得的巨大进展,自下而上或从头设计的酶设计,即在蛋白质宿主内创建全新的催化中心,可以为未来生物催化剂交付的速度和范围提供通用解决方案。如果设计要达到或甚至超过更成熟的自上而下的生物催化剂开发方法所达到的实际效用水平,那么这个研究领域现在必须解决两个核心挑战:
首先,要设计效率更接近自然系统的高活性酶。目前,即使对于相对简单的转化,也必须产生许多设计并进行实验测试,以识别出一些表现出所需活性的设计,并且需要进行广泛的进化优化以弥合与天然酶的效率差距。当针对多步反应时,设计挑战被放大,其中需要精心策划的构象调整以精确识别多种化学状态。在活性位点预组织和构象动力学之间取得平衡对于酶设计的未来成功至关重要。
其次,必须扩大从头酶可实现的化学范围,并为可大规模实施的有价值的化学过程开发催化剂。在这里,有机化学家和蛋白质设计者之间更广泛的合作对于确定合适的活性位点安排以进行新的目标转化特别有价值。通过工程化细胞翻译以将新的功能氨基酸引入蛋白质中,可以大大扩展可及化学物质的范围,这些氨基酸可用于调节金属离子辅因子的催化作用或用作小分子有机催化剂的基因编码替代物。未来,酶设计师和工程师将通过开发用于日益复杂的转化的催化剂,继续推动该领域的发展。
参考文献
1.Bailey, J. (1991). Toward a science of metabolic engineering. Science, 252(5013), 1668–1675. doi:10.1126/science.2047876
2.Cameron, D. C., & Tong, I.-T. (1993). Cellular and metabolic engineering. Applied Biochemistry and Biotechnology, 38(1-2), 105–140. doi:10.1007/bf02916416
3.Nielsen, J. (2001). Metabolic engineering. Applied Microbiology and Biotechnology, 55(3), 263–283. doi:10.1007/s002530000511
4.李国四.生物催化级联反应制备丙酮酸及L-酪氨酸衍生物[D].浙江大学,2020.DOI:10.27461/d.cnki.gzjdx.2020.003762.
5.Ricca, E., Brucher, B., & Schrittwieser, J. H. (2011). Multi-Enzymatic Cascade Reactions: Overview and Perspectives. Advanced Synthesis & Catalysis, 353(13), 2239–2262. doi:10.1002/adsc.201100256
阿拉丁:https://www.aladdin-e.com
 首页
首页 400-620-6333
400-620-6333
